基本信息
- 项目名称:
- 新型蒽环类化合物SZ-685C抗肿瘤耐药性作用机理新探索
- 来源:
- 第十二届“挑战杯”省赛作品
- 小类:
- 生命科学
- 大类:
- 自然科学类学术论文
- 简介:
- 目前临床研究发现肿瘤细胞对治疗恶性肿瘤的一线用药蒽环类化合物的耐药性已成为影响此类药物疗效的瓶颈。本研究的目的在于探索新型蒽环类化合物SZ-685C的抗肿瘤细胞耐药性的功能,并揭示其作用新机理。
- 详细介绍:
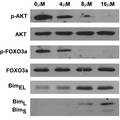
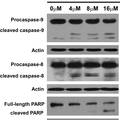
- 目前临床研究发现肿瘤细胞对治疗恶性肿瘤的一线用药蒽环类化合物的的耐药性已成为影响此类药物疗效的瓶颈。本研究的目的在于探索新型蒽环类化合物SZ-685C的抗肿瘤细胞耐药性的功能,并揭示其作用新机理。 本课题在研究证明了SZ-685C对肿瘤细胞的生长具有抑制作用的基础上,应用四甲基二氮唑蓝(MTT)比色法证明了SZ-685C能浓度依赖性抑制人阿霉素耐药肿瘤细胞株(包括人乳腺癌阿霉素耐药株细胞株MCF-7/ADR、人慢性髓性白血病阿霉素耐药细胞株K562/ADR、人急性髓性白血病阿霉素耐药细胞株HL-60/ADR)的生长。应用脱氧核糖核酸末端转移酶介导的缺口末端标记法(TUNEL)及Western-blotting技术证明了SZ-685C能有效诱导MCF-7/ADR细胞的凋亡。 同时,应用Western-blotting技术证明了SZ-685C能显著抑制耐药细胞株的AKT及其下游的FOXO3a磷酸化水平,相应的促使其下游的促凋亡蛋白Bim表达显著增高,从而可有效诱导阿霉素耐药肿瘤细胞的凋亡。 本研究的创新性在于:首次发现新型蒽环类化合物SZ-685C具有抗肿瘤耐药性的作用,并初步阐明其可能机制:SZ-685C与其他蒽环类化合物不同,能够显著下调耐药肿瘤细胞Akt的磷酸化水平,抑制Akt/FoxO信号转导通路,从而诱发耐药株肿瘤细胞的凋亡。
作品专业信息
撰写目的和基本思路
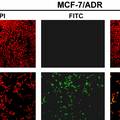
- 本课题应用MTT比色法证明了SZ-685C能浓度依赖性抑制人阿霉素耐药肿瘤细胞株的生长。应用TUNEL及Western-blotting技术证明了SZ-685C能有效诱导MCF-7/ADR细胞的凋亡。同时,应用Western-blotting技术证明了SZ-685C能显著抑制耐药细胞株的AKT及其下游的FOXO3a磷酸化水平,从而可有效诱导阿霉素耐药肿瘤细胞的凋亡。
科学性、先进性及独特之处
- 1.SZ-685C是一种新发现的蒽环类化合物,具有抗肿瘤活性,有广阔的应用前景。 2.首次发现SZ-685C与其他蒽环类化合物不同,能够显著下调Akt的磷酸化水平。 3.首次发现SZ-685C对肿瘤耐药株的抑制作用,并初步阐明其可能机制。
应用价值和现实意义
- 1.SZ-685C是一种新发现的蒽环类化合物,具有抗肿瘤活性,有广阔的应用前景。 2.首次发现SZ-685C与其他蒽环类化合物不同,能够显著下调Akt的磷酸化水平。 3.首次发现SZ-685C对肿瘤耐药株的抑制作用,并初步阐明其可能机制。
学术论文摘要
- 众所周知,蒽环类化合物是抗肿瘤的一线用药。但是,近年的临床应用和科学研究显示,部分肿瘤细胞出现了对蒽环类的耐药性。可能的耐药机制除了大家已经熟知的多药耐药基因激活之外,许多研究表明,细胞信号转导通路的异常也是重要原因之一。本研究首次发现新型蒽环类化合物SZ-685C具有抑制耐药株肿瘤细胞生长的作用,并采用MTT、TUNEL染色及Western-blotting等实验技术,对其抑制肿瘤细胞耐药株生长的机制进行了研究。结果显示,SZ-685C可以抑制Akt/FoxO通路,从而使细胞内促凋亡蛋白Bim表达升高,引发肿瘤细胞的凋亡。 本研究为该化合物最终成为新一代抗肿瘤药物提供了理论依据,以及为进一步开发高效低毒的抗肿瘤新型候选药物奠定了基础。
获奖情况
- 1.本课题组成员参与发表SCI论文一篇SZ-685C,啊marine anthraquinone,is a potent inducer of apoptosis with anticancer activity by supression of the AKT/FOXO pathway(IF:5.2,其中古明晖同学排名第三); 2.申请国家发明专利一项《蒽环类化合物在制备抗乳腺癌药物中的应用》; 3.本课题获中山大学第十一届“挑战杯”广东大学生课外学术科技作品竞赛特等奖; 4.本课题获第十一届“挑战杯”广东大学生课外学术科技作品竞赛一等奖。
鉴定结果
- 无。
参考文献
- [1] Garcia M, Jemal A, Ward EM, et al. Global Cancer Facts & Figures 2007. Atlanta, GA: American Cancer Society, 2007. [2] Jemal A, Siegel R, Ward E, et al. Cancer statistics, 2009. CA Cancer J Clin, 2009, 59(4): 225-49. [3] 孙燕.肿瘤药物治疗百年回顾与展望.中华肿瘤杂志,2004,26(11):701-703. [4] Hortobagyi GN. Anthracyclines in the treatment of cancer. An overview. Drugs, 1997, 54 Suppl 4: 1-7. [5] Gianni L, Herman EH, Lipshultz SE, et al. Anthracycline cardiotoxicity: from bench to bedside. J Clin Oncol, 2008, 26(22): 3777-84. [6] Chien AJ and Moasser MM. Cellular mechanisms of resistance to anthracyclines and taxanes in cancer: intrinsic and acquired. Semin Oncol, 2008, 35(2 Suppl 2): S1-S14; quiz S39. [7]Hortobágyi GN. Anthracyclines in the treatment of cancer. An overview. Drugs. 1997; 54 (Suppl 4): 1- 7.
同类课题研究水平概述
- 蒽环类抗生素化合物是目前临床抗肿瘤一线化疗药物,蒽环类药物无论在手术前辅助治疗、复发转移治疗和手术后辅助治疗中都占有非常重要的位置。然而癌症患者长期使用蒽环类药物出现的多耐药现象,限制了其剂量提高和临床治疗效果。因此,有必要寻找更好的结构新颖的同类型化疗替代药物。 本研究涉及的化合物SZ-685C,来自海洋红树林共生微生物的次生代谢产物,具有蒽环类化合物的基本骨架,该化合物由本课题指导老师提供。指导老师课题组已经通过体内、体外实验,研究了SZ-685C抗乳腺癌作用,并从诱导细胞凋亡、及调节细胞内信号通路等方面对其作用机理进行了探讨。结果表明,SZ-685C对于包括人乳腺癌细胞系MCF-7和MDA-MB-435在内的四种不同类型的九株肿瘤细胞系的生长均具有高效抑制作用,其抑制作用呈剂量和时间依赖性。同时,SZ-685C处理后裸鼠体内MDA-MB-435乳腺癌移植瘤的生长亦被明显抑制。 研究表明,肿瘤细胞的耐药性的产生的主要分子机制为:肿瘤细胞中的多药耐药基因表达P-糖蛋白,P-gp能引起抗肿瘤药的泵出,使肿瘤细胞内化疗药物浓度降低。而最近的研究发现,一些肿瘤细胞可以通过对负责细胞生长和凋亡的细胞信息传导通路进行调控(如PI3K/Akt通路的激活)而获得对化疗药物的抵抗力,即产生所谓的耐药性。Knuefermann等将Her2转染乳腺癌MCF-7细胞构建稳定表达Her2蛋白的细胞系,从而激活了PI3K/Akt信号转导,Akt磷酸化水平升高,最终导致肿瘤细胞对紫杉醇、多柔比星、氟尿嘧啶、鬼臼乙叉甙、喜树碱等多种化疗药的耐药。Oki等发现,胃癌患者中伴随PTEN的杂和子缺失致使Akt的磷酸化水平升高,导致对5-氟尿嘧啶、多柔比星、丝裂霉素C和顺铂的耐药,从而推测Akt的异常激活是导致胃癌细胞化疗耐药的最重要原因。Chen等研究发现,多柔比星则可能是通过激活胃癌SGC27901细胞的PI3K /Akt通路, 诱导FKHRL1磷酸化,从而影响胃癌细胞的化疗耐药性。而抑制剂wortmannin可以阻断PI3K /Akt/FKHRL1通路而提高胃癌的化疗敏感性。综上所述,化疗药物阿霉素可能是通过诱导PI3K/Akt通路的异常激活来参与癌细胞对化疗药物耐药性的产生。