基本信息
- 项目名称:
- Twist 1,MMP-2及MMP-9在肝细胞肝癌血管生成中的表达及意义
- 来源:
- 第十二届“挑战杯”省赛作品
- 小类:
- 生命科学
- 大类:
- 自然科学类学术论文
- 简介:
- 本研究拟检测97例人类肝细胞肝癌组织Twist1,MMP-2和MMP-9的表达情况,进而探讨其与MVD之间的关联性,为临床预后和抗血管生成治疗评价提供参考。
- 详细介绍:
- 上皮-见充质转变(EMT)调控因子Twist1作为bHLH家族转录因子,广泛参与了肿瘤运动,迁移和转移的生物学过程,本课题组的前期工作证明了Twist1可参与肿瘤细胞形成血管塑形过程,并与肿瘤血管生成拟态具有重要关联性意义,肿瘤细胞的运动,塑性和分泌能力与肿瘤内血管生成和微环境的建立具有重要关联性,同时引导血管内皮细胞导入也是肿瘤细胞组织生成的前提和基础。在多种成血管信号作用下,周围正常组织的固有血管向肿瘤组织内延伸并形成主要的内皮依赖性血管。本研究拟检测97例人类肝细胞肝癌组织Twist1,MMP-2和MMP-9的表达情况,进而探讨其与MVD之间的关联性,为临床预后和抗血管生成治疗评价提供参考。
作品专业信息
撰写目的和基本思路
- 在多种成血管信号作用下,周围正常组织的固有血管向肿瘤组织内延伸并形成主要的内皮依赖性血管。本研究拟检测97例人类肝细胞肝癌组织Twist1,MMP-2和MMP-9的表达情况,进而探讨其与MVD之间的关联性,为临床预后和抗血管生成治疗评价提供参考。
科学性、先进性及独特之处
- 该项目结果证明Twist1,MMP-9可由肿瘤细胞表达并促进肿瘤血管生成,这对进一步认识由肿瘤细胞本身与其构成的肿瘤局部微循环有重要意义,同时丰富了临床抗血管生成治疗的候选靶位。
应用价值和现实意义
- 该项目结果证明Twist1,MMP-9可由肿瘤细胞表达并促进肿瘤血管生成,这对进一步认识由肿瘤细胞本身与其构成的肿瘤局部微循环有重要意义,同时丰富了临床抗血管生成治疗的候选靶位。
学术论文摘要
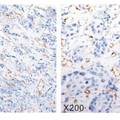
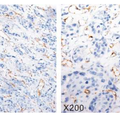
- 【摘要】目的:探讨上皮-间充质转变调控因子Twist1、基质金属蛋白酶(MMP)-2和MMP-9与肝细胞肝癌微血管密度(MVD)之间的关联性及临床病理意义。方法:收集97例肝细胞肝癌标本及临床病理资料,利用CD31标记MVD,应用免疫组织化学染色检测Twist1、MMP-2和MMP-9的表达,分析其表达与MVD、临床病理指标之间的关系。结果:MVD与病理分级和临床分期有关联性(P<0.05),Twist1浆表达、Twist1核表达、MMP-9表达阳性病例的MVD高于阴性组(P值均<0.05),对阳性病例进行Person相关分析亦证实Twist1浆表达、Twist1核表达、MMP-9表达与MVD存在关联性(P值均<0.05)。结论:肝细胞肝癌MVD增高伴随Twist1、MMP-9的高表达,这均对于提示预后不良具有一定的临床意义。 【关键词】上皮-间充质转变,基质金属蛋白酶,肝细胞肝癌,微血管密度
获奖情况
- 1.于2011年三月发表于国家综合性医药卫生类核心期刊《天津医药》(2011年3月 第39卷 第3期 193页-195页) 2.于2010年12月评定为天津医科大学大学生科研创新项目基金重点资助项目
鉴定结果
- 该生在我校病理教研室免疫组化实验室进行了为期半年的研究,对肝癌血管生成进行了病理学观察,在老师的指导下完成了科研论文
参考文献
- 1. Yang, J. and R.A. Weinberg, Epithelial-mesenchymal transition: at the crossroads of development and tumor metastasis. Dev Cell, 2008. 14(6): p. 818-29. 2. Zhao, X.L., et al., Promotion of hepatocellular carcinoma metastasis through matrix metalloproteinase activation by epithelial-mesenchymal transition regulator twist1. J Cell Mol Med, 2010. 3. Sun, T., et al., Expression and functional significance of Twist1 in hepatocellular carcinoma: Its role in vasculogenic mimicry. Hepatology, 2009.
同类课题研究水平概述
- 自Folkman提出肿瘤血管生成理论之来,抗血管生成治疗已作为基础和临床研究的热点,同时已开发出以内皮细胞为靶点的抗血管生成药并用于临床治疗中。肿瘤细胞的血管生成包括如下几种来源:(1)源于周围组织的固有血管内皮细胞的募集;(2)源于组织中或血流中的内皮细胞和间充质干细胞的分化;(3)肿瘤细胞通过塑形性改变替代内皮细胞的功能,形成肿瘤血管生成拟态。这三种肿瘤细胞相关血管内皮细胞的来源不同,前二者为宿主内皮起源,因此常规抗血管生成药物(以内皮为靶)可起效;第三者为肿瘤细胞起源,常规抗血管生成的药物治疗效果不佳,因此成为临床治疗的重要瓶颈问题。