基本信息
- 项目名称:
- 动力型锂电池用纳米片状LiCoO2材料的环保合成方法
- 来源:
- 第十一届“挑战杯”国赛作品
- 小类:
- 能源化工
- 大类:
- 自然科学类学术论文
- 简介:
- 锂电池的发展为人们提供了一种可行的电能存储方式。钴酸锂是被广泛使用的正极材料。然而,目前的材料生产技术尚不能很好地解决其在高功率动力型环境下使用的问题,并且其生产过程在能耗和环保方面存在一定问题。 本文研究了一种新的水热合成路径,用于合成有望在高倍率条件下使用的LiCoO2正极材料。现有的合成方法,主要是高温固相法,能耗较高且产物均匀性难以控制。目前被报道的水热合成方法,一般需要强碱性环境,难以达到环保的要求。我们使用双氧水代替强碱性环境,通过优化控制水热反应条件,得到了晶粒尺寸在200nm左右的LiCoO2片状纳米晶。实验表明,双氧水浓度和水热反应温度是影响生成物相纯度和晶体形貌的两个关键因素,而LiOH浓度仅对生成物形貌有微小影响。而电化学测试亦证实了合成的纯相LiCoO2纳米片具有优良的倍率特性。该水热合成路径在大规模生产中有很大的应用潜力。 我们的研究针对目前钴酸锂高倍率特性不理想的问题,将纳米科技应用于能源材料领域。不但成功得到了具有优良电化学性能的产物,也进一步验证了水热合成纳米晶体正极材料这一理念的正确性和可行性,为锂离子动力电池进一步地深入研究提供了重要参考。
- 详细介绍:
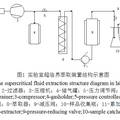
- 1.引言 目前,随着人类社会的发展,人们对于能源的需求日益增加。能源问题已经是当今世界社会上的核心问题之一。由于能源问题而衍生出的经济、环保方面的弊端已经成为人类在21世纪必须面对和解决的。传统的化石燃料,如石油、煤炭、天然气等,不可再生,并且燃烧使用时会带来空气污染,二氧化碳的排放会带来气候变化等环境问题。因此,面对这样的难题,开发清洁可再生新能源的课题担负了重要的使命,成为了人们关注的热点。 能量的储存问题是该课题的重要部分。目前,电力是应用最为广泛的二次能源,太阳能、风能、潮汐能等形式的新能源最终都是以电能的形式输出为人们所使用。但是,目前缺乏理想的存储方法。随着人们越来越迫切地希望能够为电子产品、电动工具乃至电力汽车提供切实可行的便携能源,对大容量,高功率,环保且经济的电力储存方式的需求越来越迫切。 目前市场上主要的高能小型蓄电池有镍锡电池(Ni/Cd)、镍氢电池(Ni/MH)以及各种锂离子电池(LIB),其中,锂离子电池在性能上具有显著的优越性,表现为高能量密度,长寿命,无记忆效应,环保安全等方面。因此,锂离子二次电池已经成为公认的在未来几年内可以占据主流地位的可充电电池形式。 LiCoO2(钴酸锂)由于其电容量高(140 mAhg-1)和循环性能好等特点,一直是一种广泛使用的锂离子二次电池正极材料。该化合物晶体结构为层状岩盐型,即在密排的氧原子网格上,锂离子和钴离子依次分布在相邻的(111)面上。这样的结构使得锂离子能够在晶格间迁移,因此具有很好的电化学性能。 虽然锂离子电池已经在小型电子器材上得到广泛的应用,但是由于安全性和电力输出方面的局限,该电池极少作为大功率电子设备的电源,如混合动力汽车(HEV)或电力汽车(EV)。目前一般的钴酸锂商用材料在高倍率下使用时比容量明显不佳,不能满足高功率使用时对大电流条件下电池容量的要求。因此近年来,学界已开始尝试研究改善LiCoO2高倍率电学性能的方法[4]。高倍率LiCoO2材料的出现,将会为动力型锂电池的发展和应用提供希望。 2.实验思路 2.1 材料纳米化以提升性能 目前普遍认为,考虑到正极材料在高充放电速率下的电容量与材料晶粒大小有很大关系,提升LiCoO2高倍率电学性能的有效途径之一是降低其晶粒尺寸。目前商用钴酸锂材料在高倍率(15C)下的容量衰减现象严重,50次充放电循环后其比容量仅有约80 mAhg-1,难以用于高倍率的工作环境下(相比较之下我们的样品可以在50次15C充放电循环后保持100 mAhg-1的比容量,即高倍率性能提高20%以上)。锂离子电池工作需要依靠锂离子在正极材料中嵌入、脱出以传递电荷。晶粒越小,锂离子从晶格内部扩散到晶粒表面的距离也就越短,有助于锂离子的快速迁移,有利于实现在高倍率下的高电容量[5-7]。根据Okubo等人的研究成果[4],晶粒大小为17nm左右的LiCoO2正极材料具有成为高倍率锂离子电池正极材料的潜力。由此,我们决定将材料纳米化作为提高LiCoO2正极材料高倍率电化学性能的途径。 2.2 材料合成方法的选择 目前,商用钴酸锂材料的大规模生产主要采用高温固相合成法。该方法存在很多缺点,比如难以保证反应容器内温度的均匀,材料形貌较差等等。此外,根据报道,许多液相合成方法生产LiCoO2材料已经进入了实验室阶段,如溶胶凝胶法(Sol-Gel)[8,9]、喷雾干燥法(Spraying-Drying)[10]、共析沉淀法(Co-precipitation)[11]、模板法(Post template method)[12]等等。 在Z. Peng et al 1997年发表的论文中[8],提出了一种使用溶胶-凝胶(sol-gel)法的钴酸锂制备方法。他们使用醋酸钴[Co(CH3COO)2]和醋酸锂[Li(CH3COO)2]作为原料,按1:1比例在140oC混合后溶解于柠檬酸和乙二醇中,并在170~190oC下真空干燥,形成泡沫样材料,经过数小时的煅烧后得到产物。 W. Yoon et al 在1999年报道的钴酸锂制备方法同样是使用锂和钴的醋酸盐溶于丙烯酸的水溶液后在70~80oC下搅拌形成多空的凝胶,而后干燥,预烧并在500~900oC下煅烧10小时后得到产物[9]。 此种合成法中,尽管醋酸钴和醋酸锂只需在较低的温度下混合,但所得到的泡沫样材料却需要在550oC的温度下进行煅烧数小时,能耗仍然较高;而且生产步骤较多,难以用于实际大规模生产。 Y. Li et al 在1999年报道了一种使用喷雾干燥法制备钴酸锂材料的实验方法[10]。他们同样是使用醋酸锂和醋酸钴作为原料,溶于去离子水并添加乙二醇后,用300oC气流雾化得到前驱体,而后将前驱体在800oC下煅烧4个小时得到产物。然而,用该方法制备的钴酸锂材料仍然没有体现出令人满意的高倍率特性;同时800oC的煅烧温度对设备要求高,能耗大。 F. Jiao et al在2005年采用模板法制备得到了多孔的纳米线状钴酸锂[12]。他们采用多孔的硅材料作为模板,在其中注入硝酸钴的乙醇溶液并煅烧,得到了具有纳米线状结构的Co3O4,而后将其与氢氧化锂在400oC下煅烧得到产物(低温LiCoO2)。缺点:合成步骤多,只是用于小规模实验性研究,无法应用于实际大规模生产,煅烧温度较高,且产品电化学性能较差(比容量小于100mAhg-1)。 H. Chen et al在2002年报道了一种采用共析沉淀法制备纳米级钴酸锂材料的方法[11]。他们采用锂和钴的硝酸盐作为原料,配比中锂略微过量。将原料溶解后的溶液以适当速率滴加入3M 的KOH乙醇溶液中,可以观察到深色沉淀。离心分离后干燥煅烧(400oC, 500oC, 600oC, 700oC)10小时以后得到产物。同样,这种方法中干燥煅烧温度高且时间长,能耗大。 S. Chang et al在2001年报道了一种采用水热合成法制备钴酸锂的试验方法[16]。他们将氢氧化锂和氢氧化钴溶解于12M KOH溶液中,而后在130 oC~200 oC下水热反应。上面两种方法的问题在于强碱性下合成,环境不友好,阻碍了工业推广。 在众多合成方法中,水热合成法公认为是一种比较适于晶粒生长,易于控制形貌的合成方法。从水热合成法的众多应用中,我们也发现这种方法可以方便地控制生成单晶的粒径,获得纳米材料。此外,水热合成法相比较与高温固相法,具有反应温度较低、反应均匀充分的优点,在未来的大规模生产中可以有效地控制能耗,并且保证产品质量的稳定性。因此我们决定以水热合成法作为我们制备方法的首选。 已有研究表明,水热合成法[13-15]能够得到纯相的HT-LiCoO2晶体。Chang等人报道了一种水热合成LiCoO2纳米晶的方法,水热反应溶液为Ca(OH)2和LiOH的混合溶液,以及高浓度的碱溶液[16]。反应得到晶粒尺寸100nm左右的HT-LiCoO2粉末,以这种纳米晶制成的正极材料体现出很好的电化学性能。然而,由于这种方法使用了大量的碱溶液(12M KOH),必须考虑如何在水热合成结束后去除这些碱溶液。这可能会对该方法应用于商业生产产生障碍。因此,必须对这种合成路径进行一些改进,使其能够应用于大规模生产。 针对目前上述方法的缺点,我们提出了一种新的水热合成方法。该方法使用H2O2作为氧化剂代替碱性环境,促使Co2+被氧化成Co3+,通过水热合成得到LiCoO2片状纳米晶。采用双氧水替代强碱性环境,使得生产过程更加安全、环保。采用这种方法,在未来的工业生产中,避免了强碱性工业废水带来的环境问题。 2.3 优化反应条件 我们通过优化一系列反应参数,详细研究各种反应条件对结果的影响,得到了形貌和粒径俱佳的纯相LiCoO2晶体。在本文中,我们将详细讨论水热环境对相纯度和晶体形貌的影响。电化学测试表明,由本文中方法得到的尺寸为200nm的纳米片在高倍率条件下电化学性能优良,具有很大的应用潜力和商业价值。 3.实验过程 3.1 水热合成LiCoO2纳米晶体 通过水热反应合成LiCoO2粉末。反应物为分析纯CoCl2•6H2O、LiOH•H2O、H2O2,设想在水热过程中将发生如下反应: 2CoCl2 + H2O2+ 6LiOH → 2LiCoO2+ 4LiCl+ 4H2O (1) 具体的实验步骤为:将一定量的CoCl2•6H2O溶解于去离子水中,超声波分散处理后加入 H2O2溶液,充分搅拌5分钟。在搅拌条件下缓慢滴入LiOH溶液,将得到的粉红色悬浊液移入特氟隆密封高压反应釜,放入电炉中在一定温度下加热反应一段时间。反应结束后,将得到的黑褐色产物用去离子水洗涤后抽滤,放入60oC烘箱中干燥过夜。实验流程如图1所示。 3.2 合成LiCoO2纳米晶体的表征 得到的产物粉末将采用多种方法进行表征。相组成将通过XRD测定,X光衍射测定的参数为:仪器型号D/max2550,Cu Kα射线,步长0.02°,2θ角范围为10-70°,在室温下测量。通过软件Jade 7.0对衍射结果进行分析,确定相组成。生成物形貌将通过SEM和TEM予以检验,采用FEI SIRION 200和JEOL JEM-2100F(200kV)。同时使用等离子发射光谱仪(ICP)X射线光电子能谱仪(XPS)确定生成物纯度和化学价。 3.3 LiCoO2纳米晶体的电化学测试 我们测定合成得到的LiCoO2正极材料实际电化学性能的主要方法是通过组装成标准纽扣电池在电化学测试仪上进行测试。我们将水热反应得到的LiCoO2粉末与乙炔黑和聚偏二氟乙烯(PVDF)按质量比60:25:15溶于有机溶剂N-甲基吡咯烷酮(NMP),作为锂电池正极。一般情况下,商用锂离子电池仅含5%左右的导电材料。但是在本研究中,制得电池旨在评估LiCoO2纳米晶体的高倍率特性,因此采用了较大量的乙炔黑以提升电极导电性。混合物用磁力搅拌子搅拌过夜,以使其充分混合,最终得到黑色浆料。将浆料涂覆于铝箔上,90oC干燥6小时,然后将干燥后的薄膜置于真空烘箱中80oC干燥过夜,作为纽扣电池的正极材料。纽扣电池以正极为工作电极,金属锂为负极。充放电平台为充电4.5V、放电2.5V。 4. 结果与讨论 4.1 H2O2浓度对产物相组成的影响 我们尝试了一系列试验参数以得到纯相的LiCoO2。根据其他人的研究报告,水热合成的LiCoO2纳米晶粒的形貌和相纯度主要受如下四个因素的影响: H2O2浓度,水热合成温度,Li/Co比,以及反应时间。为实验简便起见,对实验结果影响最小的因素并没有列入我们的考虑范围。根据原来水热法合成LiMnO2正极粉末材料的经验,我们认为当水热合成的时间足够时,产物的相组成并不会变化[17,18]。因此,我们决定将反应时间定为20小时,以保证水热反应完全。所以在实验中我们研究其余三个因素的影响,即H2O2浓度,水热合成温度和Li/Co比。 我们首先考虑了H2O2浓度的影响。为了说明这个因素的影响效果,我们选取5个具有代表性的试样作为例子,它们都除了H2O2浓度外,其他合成条件完全相同。所有的5个试样都在200oC下反应,并且Li/Co比为4:1。然而,随着双氧水浓度的不同,反应结果也大相径庭。请参见表1。 图3显示了这些试样的XRD图谱,显示出H2O2浓度对试样相组成的影响。理论上,根据反应方程(1),0.005molH2O2足够与0.01molCoCl2反应生成LiCoO2。然而,实验结果表明,这么多的H2O2却不足以得到纯相的LiCoO2。根据如图2所示XRD图谱,当H2O2浓度为6.25 vol%时,反应没有得到LiCoO2。当H2O2的浓度达到25 vol%时,也只能检测到很少的LiCoO2。当H2O2浓度达到50vol%时,我们可以得到纯净的试样。这些结果表明H2O2浓度对水热法合成的试样的相组成有很大影响。在水热合成中,H2O2的作用是把Co2+氧化成Co3+的氧化剂。因为这种氧化反应很难在稀溶液中发生,所以H2O2的浓度很重要。根据我们的实验结果, H2O2浓度为6.25 vol%时无法发生这种氧化反应,因此此时最终产物中的主要的相是Co(OH)2。随着H2O2浓度的增大,相组成发生相应的变化。这表明除了反应方程(1)所代表的反应,亦发生了其他反应: CoCl2 + 2LiOH → Co(OH)2+ 2LiCl (2) CoCl2 + 2LiOH → CoO + H2O + 2LiCl (3) 3CoCl2 + H2O2 + 6LiOH → 6LiCl + Co3O4 + 4H2O (4) 图2 不同双氧水浓度下得到的产物的XRD衍射峰图,表示H2O2浓度对合成产物相成分的影响 样品编号 H2O2 vol % 反应温度 (oC) Li/Co比 产物组成 推测所发生的反应 S1 6.25 200 4:1 Co(OH)2+CoO+Co3O4 2, 3, 4 S2 12.5 200 4:1 CoO+Co3O4 +Co(OH)2 2, 3, 4 S3 25 200 4:1 Co3O4 +LiCoO2+CoO 1, 3, 4 S4 37.5 200 4:1 Co3O4 +LiCoO2+CoO 1, 3, 4 S5 50 200 4:1 LiCoO2 1 S6 50 160 4:1 LiCoO2 +Co3O4 1, 4 S7 50 180 4:1 LiCoO2 +Co3O4 1, 4 S8 50 220 4:1 LiCoO2 +Co3O4 1, 4 S9 50 200 3:1 LiCoO2 1 S10 50 200 6:1 LiCoO2 1 S11 50 200 8:1 LiCoO2 1 表1 选用不同水热合成实验参数制备的LiCoO2纳米晶体的成分分析 4.2 H2O2浓度对产物形貌的影响 我们通过SEM和TEM表征产物形貌,结果如图3所示。图3a至图3d分别是样品S2、S3、S4、和S5的SEM扫描结果。可以看出,双氧水浓度的变化不但改变了产物的化学成分,对产物形貌的影响是非常明显的。样品S2、S3、S4呈无定形态,而S5却呈典型的片状。晶体形貌的不同可以由合成晶体的微观结构不同来解释:S2、S3、S4、S5的主要组成相分别为CaO、Ca3O4、Ca3O4和LiCoO2;CoO和Ca3O4晶体属于立方晶系,无定形态为其晶粒的一种典型形态;LiCoO2属于六方晶系,晶粒经常呈片状。样品S5的TEM照相结果如图3e所示,呈明显片状。图3f展示了S5的某个单晶纳米片,研究人员对该纳米晶粒进行了进一步的电子衍射和高分辨透射电镜(HRTEM)表征。电子衍射花样如图3g所示,呈典型的从[001]方向观察的六方晶系结构,表明了晶粒的内部结构。HRTEM的表征结果如图 3h所示,照片中可以观察到明显的片状纳米晶的一系列边缘,边缘间距为0.14nm,正好等于六方晶系(110)晶面间距。照片右下角小图是LiCoO2晶体从[001]轴观察的模拟图,(110)面的间距已被确定。以上结果表明产物形成该结构是由于晶体沿ab面[(001)面]的生长倾向,这正是六方晶系典型的生长特点。 4.3 水热合成温度对相纯度和晶体形貌的影响 水热合成温度是另外一个对LiCoO2其重要作用的因素。图4表明在不同温度下制备的试样的XRD图谱。如图4所示,在低温(160oC)下反应时,产物中Co3O4是主要的相成分。随着水热合成温度的上升,LiCoO2逐渐成为主要的成分。当水热合成温度升至200oC时,我们得到纯净的LiCoO2。然而,当温度继续升至220 oC,Co3O4相又再次出现了。这种现象表明LiCoO2的水热合成过程非常复杂。在我们的实验中,水热合成纯净的LiCoO2的合适温度是200 oC。在LiCoO2复杂的水热合成过程中,有两个过程,即从Co2+到Co3+的氧化过程和锂离子的嵌入过程,对相转变起到了重要作用。一般认为,水热合成温度越高,越利于氧化反应的发生,但可能会对锂离子嵌入过程的发生有一定负面作用。水热合成温度的升高会使反应的压力有很大增高(在180 oC,200 oC和220 oC时的压力分别为1MPa,1.45MPa和2.35MPa)。 反应环境压力的升高对层状LiCoO2 (C轴取向)的合成没有帮助,因为在高压下,晶体倾向于生成小晶格参数的密堆结构。因此,在高压高温下,LiCoO2晶体并不十分稳定,倾向于生成小晶格参数的相,比如Co3O4。当然这个过程的机制十分复杂,需要更进一步的实验结果来支持这个假设。 图3 不同HwOw浓度下合成得到粉体的形貌变化:(a)样品S2;(b)样品S3;(c)样品S4;(d)样品S5;(e)样品S5纯相LiCoO2的TEM图像;(f)样品S5的高分辨透射电镜图像体现出其六方晶格构造,右下角小图为六方晶格原子结构的图示([001]晶带轴)。 图4 不同温度下制备的水热产物的XRD测试结果,表现出水热合成温度对产物相组成的重要影响,同时也可看出最适宜的水热温度为200 oC。 通过SEM,我们可以观察到在不同温度制备的试样的晶体形貌。图5a到图5d就是在160 oC到220 oC不同温度合成的试样的显微图像.只有在200 oC时合成的试样表现出了平板状的形状。这与在图3中的结果相一致。只有在200 oC时和车的试样是纯相的六方LiCoO2,其他都含有一些立方Co3O4相。这些结果进一步证明了水热合成粉体的晶粒形状受相组成的影响。平板状的晶粒只能在水热反应条件合适于合成LiCoO2纯相的时候得到。 图5 不同温度下得到的LiCoO2粉体的SEM图像: (a)160 oC;(b)180 oC;(c)200 oC;(d)220 oC。 可以看出温度对晶体形貌有明显的影响。 4.4 Li/Co比例的影响 之前的研究报告表明[14-16],Li/Co比对产物相纯度有着极为重大的影响。因此在本项目的实验中,研究人员亦考虑了该因素。图6是以不同Li/Co比例合成得到的样品的XRD图样(其他参数保持不变)。令研究人员感到意外的是,各种反应物比例都能够得到纯相的LiCoO2,并且SEM亦显示所有样品均为片状纳米晶体。以上发现表明,至少在本研究中,Li/Co比例并不是水热合成结果的决定性因素。不过,XRD衍射峰强度的不同还是表明,Li/Co比例对生成物晶粒的尺寸或许存在影响。随着Li/Co比例的增加,晶粒尺寸相应减小。本研究结果与之前Chang等人的报道[16]颇有不同。首先,本研究证明LiCoO2能够在碱浓度相对较低的水热环境中合成;其次,增加LiOH浓度仅对产物尺寸存在有限的影响,而对相纯度无明显影响。在本研究小组设计的水热反应路径中,完全不需要强碱环境。由于提供了一个更为方便安全的水热反应环境,该发现对将来的大规模生产有重要意义。 图6 不同Li/Co比例下合成产物的XRD测试结果。所有样品均得到纯相LiCoO2。不同峰强以及不同的半峰宽度是由于晶粒尺寸的差异所造成。 4.5 等离子发射光谱(ICP)和X射线光电子能谱(XPS)的纯相表征测试 为了进一步确定物质的化学纯度以及元素的氧化态,我们将所制备的纳米片状结构的样品进行了等离子发射光谱(ICP)以及X-光电子能谱(XPS)的测试。通过ICP测试所得到的化学分析结果列于表2,从化学计量结果可以看出物质为接近纯相的LiCoO2。物质中主要的元素为Li和Co,其他均为微量元素。这些微量元素的产生主要是由于在水热合成以及后续处理的过程中引入的。相对较高含量的元素诸如Na,Ca,K和Si被检测到的原因主要是由于在溶解粉末的时候加入了氢氟酸 (HF)。这里所得到的Li/Co摩尔比为0.981,此结果非常接近理论值。因此从ICP的结果表明试验所制备得到的是纯相的LiCoO2。 表2 样品S5纳米片状LiCoO2粉体的元素组成(质量分数) XPS光谱的结果示于图7,从图中可以看出C,O,Co的尖峰被检测到。C的1s峰位于284.6eV,这是由于吸收了周围的CO和COO阴离子所导致的碳污染[19]。尖峰的位置十分稳定,因此可以用于标定其他峰的位置。 为了确认Co,O以及Li的化合价,我们对Co的2p轨道,O的1s轨道以及Li的1s轨道的发射谱进行了精确的标定。对于化学计量比的LiCoO2,一般的氧化态为Co3+,O2-,Li+ [20]。对于我们的样品而言,Co的2p轨道的芯能级包括自旋轨道的分裂:Co的2p轨道3/2位于779.3eV而有1/2位于794.2eV。此结果证明Co离子的价态为3+。对于O的1s轨道,位于529eV的主峰对应于O2-离子。Li 1s轨道的发射谱位于图6右上方的插入图。Li 1s轨道的光电子发射线呈现出一个非常弱而且宽的峰,此峰与Co的3p峰相似。Li的1s轨道的键能为54.2eV,此结果表明Li粒子位于氧原子的正八面体当中[20]。 图7 水热制备纯相LiCoO2晶体的XPS测试结果;所有的峰均得到确认。右上角的小图体现了Li+处于八面体间隙之中。 4.6 纯相LiCoO2的电化学性能测试 所制备的纳米LiCoO2的电化学行为表征是通过测试使用200nm尺寸的LiCoO2纳米片所制备的纽扣电池的电学性能来实现的。测试结果如图8所示。图8a、图8b、图8c表示在1C、5C以及15C的放电倍率下LiCoO2在前10个充放电循环下的容量情况。全部的50个循环下的表征结果如图8d所示。值得注意的是在相对较低的倍率下(1C和5C)容量比较稳定。在1C的倍率下电池容量能够在50个循环以后维持在138 mAhg-1,在5C的情况下此值为123 mAhg-1。另外在此过程中仅有大约10 mAhg-1的容量衰减。在高放电倍率(15C)下经过50次充放电循环容量从134 mAhg-1下降到103 mAhg-1。显然更高的放电倍率会使得容量下降的越快。尽管在高倍率下电池的容量下降的较低倍率下来说快很多,但它仍然能够稳定在100 mAhg-1这样一个能够考虑投入实际使用的水平。 与Okubo[4]等人所采用的控制尺寸的方法相比,高放电倍率下电容量的提高是十分明显的。在他们的报道中,在10C的倍率下经过20次循环,晶粒尺寸为17nm和8nm的电池容量分别下降为80 mAhg-1和34 mAhg-1。 而我们的方法所制得的样品尺寸大约为200nm,并且能够在15C放电倍率的条件下维持107 mAhg-1。此结果表明一个合适的晶体尺寸能够决定电池的倍率特性。两种方法的不同亦揭示了纳米片状的LiCoO2在高倍率充放电情况下使用的巨大潜力。 图8 纳米片状钴酸锂(晶粒大小约200nm)的电化学性能。(a)在1C充放电速率下循环10次;(b)在5C充放电速率下循环10次;(c)在15C充放电速率下循环10次;(d)50次充放电循环的倍率特性。 5. 结论 从以上的结果讨论中可以看出,在优化的水热合成参数条件下,我们能够重复稳定地制备得到具有200nm层片状结构的LiCoO2晶体。H2O2的浓度以及水热合成的温度是决定相纯度以及晶体形貌的两大决定因素,与此同时LiOH的浓度仅对晶体的尺寸有较弱的影响。电化学性能的测试揭示了采用这种方法合成的LiCoO2具有良好的倍率特性,可以考虑作为动力型锂电池的正极材料使用。 在这研究中,我们提出了一种新的水热合成LiCoO2正极材料的方法。我们采用水热合成法代替传统的高温固相合成,降低了能耗,保证了材料性能的稳定性。相对于已有报道的水热合成方法,我们的方法避免在高碱性环境下制备材料,解决了环保的问题。该方法符合国家有关政策对节能减排方面的引导,并且易于大规模生产,具有巨大的商业应用前景。目前我们正在积极申报有关专利,并正与相关厂家洽谈合作,争取尽早将该方法投入商业生产环节。
作品专业信息
撰写目的和基本思路
- 通过对文献的研究,我们认为要提升LiCoO2材料的高倍率特性,关键在于得到晶粒细小的单晶颗粒。因为LiCoO2晶格内部存在锂离子通道,如果能够得到纳米级的单晶颗粒,那么锂离子迁移时将大大加快锂离子在正极材料中的脱嵌和嵌入,进而提升材料的电化学性能。 基于这个思想,我们决定采用水热合成的方法得到符合预期的材料。
科学性、先进性及独特之处
- 该研究方法已经见诸文献报道,科学家们通过制备纳米级正极材料,在一定程度上提升了电池的高倍率特性。 目前文献所述的水热法合成LiCoO2的方法中反应环境比较苛刻,一般需要很高的碱性。我们创造性地使用一定浓度的氧化剂(H2O2)替代碱液,以更加清洁环保的方法得到高纯度的LiCoO2纳米晶体。具有比以往研究更高的实用价值。并且经过电化学测试,该合成方法对材料电化学性能的提升是极为可观的。
应用价值和现实意义
- 本研究组所设计的合成路径,不但能够得到高纯度LiCoO2晶体,并有效控制LiCoO2晶粒形貌方法简单,而且成本、能耗较低,具有很高的实际应用潜力。组装电池实测表明,合成的LiCoO2材料有很好的电学性能,尤其是在高倍率条件下,比容量相较以往类似合成方法提升30%以上,而且体现出很好的稳定性,已经具备了一定的实际应用价值。
学术论文摘要
- 本文记录了一种新的水热合成路径,用于合成有望在高倍率条件下使用的LiCoO2正极材料。通过控制水热反应条件,得到了晶粒尺寸在200nm左右的LiCoO2片状纳米晶。实验表明,双氧水浓度和水热反应温度是影响生成物相纯度和晶体形貌的两个关键因素,而LiOH浓度仅对生成物形貌有微小影响。而电化学测试亦证实了合成的纯相LiCoO2纳米片具有优良的倍率特性,表明该水热合成路径在大规模生产中有很大的应用潜力。
获奖情况
- 2009年2月25日,该论文Preparation of LiCoO2 Nano Plates via Hydrothermal Routine and the Investigation of Their Electrochemical Behavior at High Rates在国际学术期刊Nanotechnology(英国物理学会下属期刊,影响因子3.31,SCI/EI全文检索)上正式发表。20卷11期,文献编号 115608
鉴定结果
- 本项目组同学展开了近两年的研究,经过反复试验和充分论证,取得了可喜的技术突破,并在国际知名学术刊物上发表了作品。该研究是纳米技术应用于锂离子电池研究的成功范例,为动力型锂电池的实际应用提供了重要参考。
参考文献
- 1、Garcia B., Farcy J., Pereira-Ramos J. P., Baffier N., Electrochemical Properties of Low Temperature Crystallized LiCoO2, J. Electrochem. Soc. 144 (1997) 1179. 2、Okubo M., Hosono E., J. Kim, Enomoto M., Kojima N., Kudo T., Zhou H. S., Honma I., Nanosize Effect on High-Rate Li-Ion Intercalation in LiCoO2 Electrode, J. Am. Chem. Soc., 129 (2007) 7444. 3、Liu Q., Mao D. L., Chang C. K., Huang F. Q., Phase conversion and morphology evolution during hydrothermal preparation of orthorhombic LiMnO2 nanorods for lithium ion battery application, J. Power Sources, 173 (2008) 538. 4、Chang S. K., Kweon H. J., Kim B. K., Jung D. Y., Kwon Y. U., Syntheses of LiCoO2 for cathode materials of secondary batteries from reflux reactions at 130–200 °C, J. Power Sources, 104 (2002)125.
同类课题研究水平概述
- 二次锂离子电池是以两种不同的能够可逆地插入及脱出锂离子的嵌锂化合物分别作为电池的正极和负极的二次电池体系,充电时锂离子从正极材料的晶格中脱出经过电解质后插入到负极材料的晶格中,使得负极富锂,正极贫锂;放电时锂离子从负极材料的晶格中脱出,经过电解质后插入到正极材料的晶格中,使得正极富锂,负极贫锂。这样正负极材料在插入及脱出锂离子时相对于金属锂的电位差值就是电池的工作电压。LiCoO2晶体结构为层状岩盐型,即在密排的氧原子网格上,锂离子和钴离子一次分布在相邻的(111)面上。这样的结构使得锂离子能够在晶格之间迁移,因此具有十分优良的电化学性能。目前几乎所有的小型电子元件都是采用的LiCoO2锂离子电池。虽然锂离子电池已经在小型电子器材上得到了广泛的应用,但是由于安全性和电力输出方面的局限,该电池极少作为大功率电子设备的电源,如混合动力汽车(HEV)或电力汽车(EV)。 正极材料的发展比较缓慢,成为制约锂离子电池整体性能进一步提高的关键因素,为了提高锂离子电池性能,降低成本,锂离子电池征集材料的研究非常活跃。LiCoO2由于比容量高达140mAh/g左右,并有较好的循环性能和安全性,且较易制备,因而成为目前唯一已经大量用于生产的锂离子电池正极材料,LiNiO2,LiMn2O4等替代材料仍旧处于研究阶段。 最近,学界已经开始尝试研究LiCoO2的高倍率电化学性能,目前普遍认为,要想提升LiCoO2的电化学性能,关键在于实现对材料的晶体形貌控制,以得到细小晶粒的LiCoO2的正极材料。正极材料在高充放点速率下的电容器与材料晶粒的大小有很大关系。因为晶粒越小,锂离子在晶格内扩散的距离也就越短,有助于锂离子的高速迁移,从而实现在高倍率下电池仍旧具有较高的电容量。 Chang 等人报道了一种水热合成LiCoO2 纳米晶的方法,水热反应溶液为Ca(OH)2和LiOH的混合溶液,以及高浓度的碱溶液。反应得到晶粒尺寸100nm左右的HT- LiCoO2粉末,以这种纳米晶制成的正极材料具有良好的电化学性能。然而,由于这种方法使用了大量的碱溶液(12M KOH),因此在制备过程中必须考虑如何在水热合成结束以后去除这些碱溶液。这可能会对该方法应用与商业生产产生障碍。因此,必须对这种合成路径进行一些改进,使其能够应用与大规模生产。